Физики из МФТИ научились уничтожать тромбы при помощи лазера
Лазеры в медицине, Новости науки и техники 23.10.2017 Комментариев к записи Физики из МФТИ научились уничтожать тромбы при помощи лазера нетФизики из США, Германии и России разработали технологию, позволяющую находить и уничтожать «беглые» тромбы в сосудах, не вскрывая тело человека, при помощи лазерного луча, и опубликовали ее описание в журнале PLoS One.
«Мы показали, что при помощи метода фотоакустической проточной цитометрии можно обнаружить тромбоэмболы в потоке крови. Потенциально существует возможность тут же уничтожать обнаруженный сгусток, но это тема следующего исследования», — заявил Александр Мелерзанов, декан факультета биологической и медицинской физики МФТИ, чьи слова передает пресс-служба института.
Real-Time Label-Free Embolus Detection Using In Vivo Photoacoustic Flow Cytometry
Thromboembolic events are one of the world’s leading causes of death among patients. Embolus or clot formations have several etiologies including paraneoplastic, post-surgery, cauterization, transplantation, or extracorporeal circuits. Despite its medical significance, little progress has been made in early embolus detection, screening and control. The aim of our study is to test the utility of the in vivo photoacoustic (PA) flow cytometry (PAFC) technique for non-invasive embolus detection in real-time. Using in vivo PAFC, emboli were non-invasively monitored in the bloodstream of two different mouse models. The tumor-free mouse model consisted of two groups, one in which the limbs were clamped to produce vessel stasis (7 procedures), and one where the mice underwent surgery (7 procedures). The melanoma-bearing mouse model also consisted of two groups, one in which the implanted tumor underwent compression (8 procedures), and one where a surgical excision of the implanted tumor was performed (8 procedures). We demonstrated that the PAFC can detect a single embolus, and has the ability to distinguish between erythrocyte–rich (red) and leukocyte/platelet-rich (white) emboli in small vessels. We show that, in tumor-bearing mice, the level of circulating emboli was increased compared to tumor-free mice (p = 0.0013). The number of circulating emboli temporarily increased in the tumor-free control mice during vessel stasis (p = 0.033) and after surgical excisions (signed-rank p = 0.031). Similar observations were noted during tumor compression (p = 0.013) and after tumor excisions (p = 0.012). For the first time, it was possible to detect unlabeled emboli in vivo non-invasively, and to confirm the presence of pigmented tumor cells within circulating emboli. The insight on embolus dynamics during cancer progression and medical procedures highlight the clinical potential of PAFC for early detection of cancer and surgery-induced emboli to prevent the fatal thromboembolic complications by well-timed therapy.
http://journals.plos.org/plosone/article?id=10.1371%2Fjournal.pone.0156269
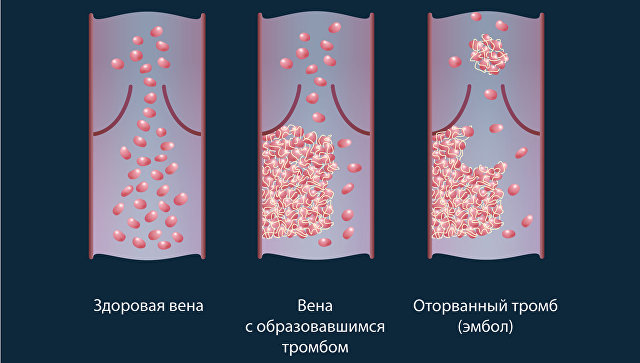
Одной из главной причин возникновения инсультов и инфарктов и связанной с ними смерти человека является формирование тромбов на стенках артерий и вен, которые периодически «отваливаются» и начинают путешествовать по кровеносной системе. Часто такие «беглые» тромбы закупоривают сосуды, что приводит к смерти или кислородной смерти отдельных органов или тканей.
Несмотря на серьёзность проблемы, на данный момент высокочувствительные способы ее диагностики пока не созданы. Методы, используемые сейчас, имеют низкую чувствительность и не позволяют уничтожать тромбы в режиме реального времени.
Мелерзанов и его коллеги из университета штата Арканзас (США) и университетов Франкфурта восполнили этот недостаток, научившись наблюдать за тромбами при помощи методики так называемой фотоакустической проточной цитометрии.
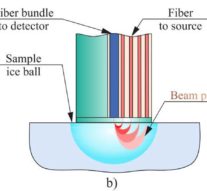
Ее идея заключается в следующем – в организм вводятся клетки, наполненные специальным светящимся веществом, за распространением которого ученые могут следить, облучая ту или иную часть тела при помощи лазера, который заставляет молекулы красителя светиться на определенной длине волны.
Наблюдая за интенсивностью свечения краски в разных частях сосуда, ученые могут определять, присутствуют ли в кровотоке крупные включения в виде тромбов, определять их тип и даже уничтожать их при помощи лазера. Работу этой методики физики из РФ и стран Запада проверили, наблюдая за образованием тромбов в сосудах мышей.
Кроме того, вместо краски можно использовать сами красные кровяные тельца, содержащие в себе пигмент гемоглобин, который тоже может поглощать лучи лазера и испускать их обратно на другой длине волны. Наблюдая за этим «кровяным излучением», ученые могут определять, где наблюдается опасное скопление эритроцитов, указывающее на формирование тромба, или где их нет, что говорит о наличии лейкоцитарного тромба.
Как отмечает ученый, применение этой техники в реальном времени на крупных сосудах во время операции пока что является сложной задачей. Однако то, что данный метод позволяет отслеживать факт появления «беглых» тромбов во время медицинских процедур и в постоперационном периоде, в том числе при развитии рака, позволяет надеяться, что в будущем он поможет предотвратить развитие осложнений, связанных с тромбами, на ранних стадиях их появления.



Leave a comment
You must be logged in to post a comment.